- Електрохимия и галванични покрития
- Процесът на електролиза или зареждане на батерията
- галванотехника
- В електрониката
- заключение
Помогнете на развитието на сайта, споделяйки статията с приятели!
Сред термините в електриците има такива понятия като анод и катод. Това се отнася за източници на енергия, галванични покрития, химия и физика. Терминът се намира и във вакуумната и полупроводникова електроника. Те обозначават констатациите или контактите на устройствата и какъв електрически знак притежават. В тази статия ще ви кажем какви са анодите и катодите и как да определите къде са в електролизера, диода и батерията, кои от тях са плюс и минус.Електрохимия и галванични покрития
В електрохимията има два основни раздела:
- Галванични клетки - производството на електроенергия поради химическа реакция. Тези елементи включват батерии и акумулаторни батерии. Те често се наричат химически източници на ток.
- Електролиза - въздействието върху химическата реакция на електричеството, с прости думи - с помощта на източник на енергия, се предизвиква някаква реакция.
Помислете за окислително-редукционна реакция в галваничната клетка, тогава какви процеси се провеждат при електродите й?
- Анод - електродът, върху който има окислителна реакция, тоест, той се отказва от електрони. Електродът, върху който протича окислителната реакция, се нарича редуциращ агент.
- Катодът е електрод, върху който протича реакция на редукция, т.е. приема електрони. Електродът, върху който протича реакцията на редукция, се нарича окислител.
Това повдига въпроса - къде е плюсът и къде е минусът на батерията? Въз основа на дефиницията, анодът дава електрони на галваничната клетка.
Важно е! В ГОСТ 15596-82 е дадена официална дефиниция на наименованията на заключенията на химическите източници на ток, ако е накратко, след това плюс на катода и минус на анода.
В този случай се разглежда потокът на електрически ток през проводника на външната верига от окислителя (катода) към редуктора (анода). Тъй като електроните във веригата протичат от минус до плюс, а електрическият ток е обратното, то катодът е плюс, а анодът е минус.
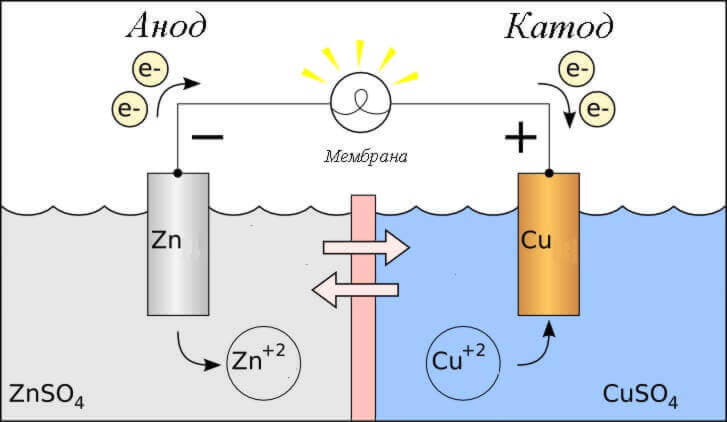
Внимание: токът винаги се влива в анода!
Или същото на диаграмата:

Процесът на електролиза или зареждане на батерията
Тези процеси са сходни и противоположни на галваничната клетка, тъй като не енергията идва от химична реакция, а обратното - химическа реакция се дължи на външен източник на електричество.
В този случай, плюс захранването, всичко се нарича също катод и минус анода. Но контактите на акумулаторната галванична клетка или електродите на електролизера вече ще имат противоположни имена, да видим защо!
Важно е! Когато галваничната клетка се разрежда, анодът е минус, катодът е плюс, когато се зарежда, е обратното.
Тъй като токът от положителния изход на захранващия източник отива към положителния изход на батерията, последният вече не може да бъде катод. Позовавайки се на горното, може да се заключи, че в този случай електродите на батерията условно сменят местата си при зареждане.
След това през електрода на акумулаторна галванична клетка, в която протича електрически ток, се нарича анод. Оказва се, че при зареждане на батерията, плюс става анод, и минус катода.
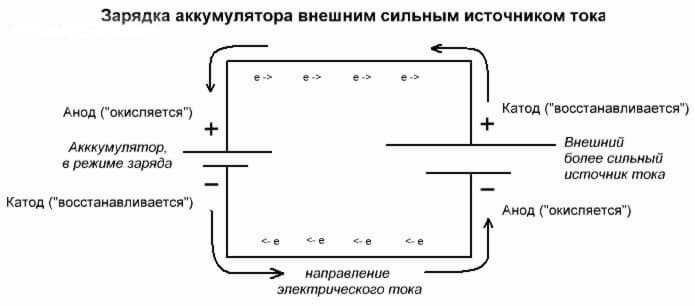
галванотехника
Процесите на отлагане на метали в резултат на химическа реакция под въздействието на електрически ток (по време на електролиза) се наричат галванични. Така светът получи сребърно, позлатено, хромирано или друго покритие от метал и части. Този процес се използва както в декоративни, така и в приложни цели - за подобряване на корозионната устойчивост на различните компоненти и възли на механизмите.
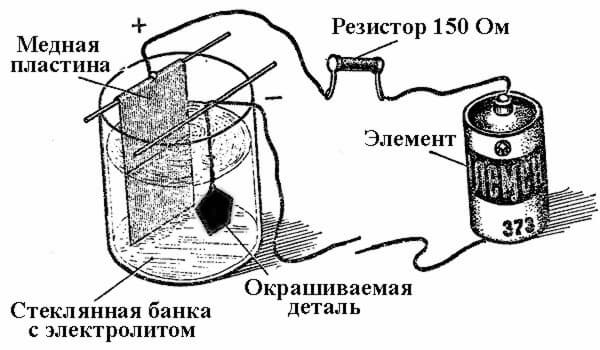
Принципът на работа на съоръженията за нанасяне на галванични покрития е в използването на солеви разтвори на елементите, с които частта ще бъде покрита като електролит.
При галванопластиката анодът е също електрод, към който е свързан положителният изход на захранващия източник, съответно катодът в този случай е минус. В този случай, металът се отлага (редуцира) върху отрицателния електрод (редукционна реакция). Тоест, ако искате да направите позлатен пръстен със собствените си ръце, свържете отрицателния кабел на захранването към него и го поставете в контейнер с подходящия разтвор.
В електрониката
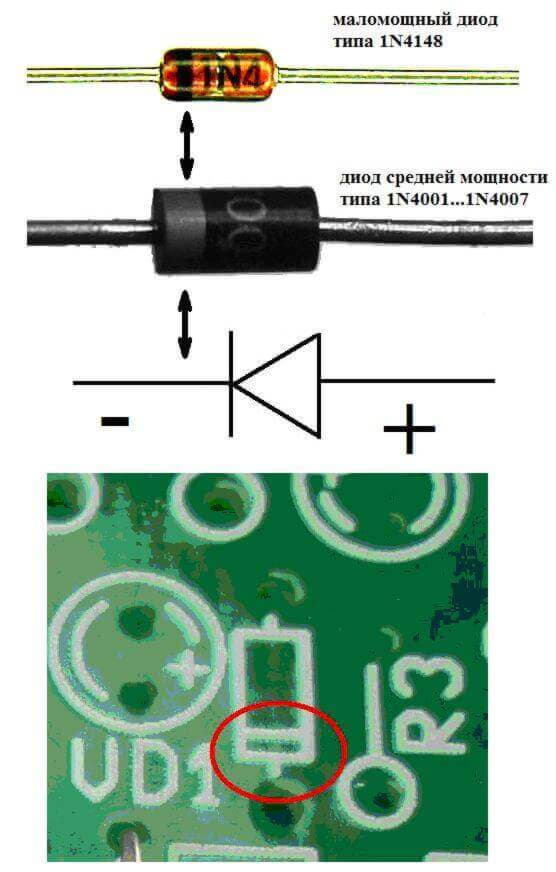
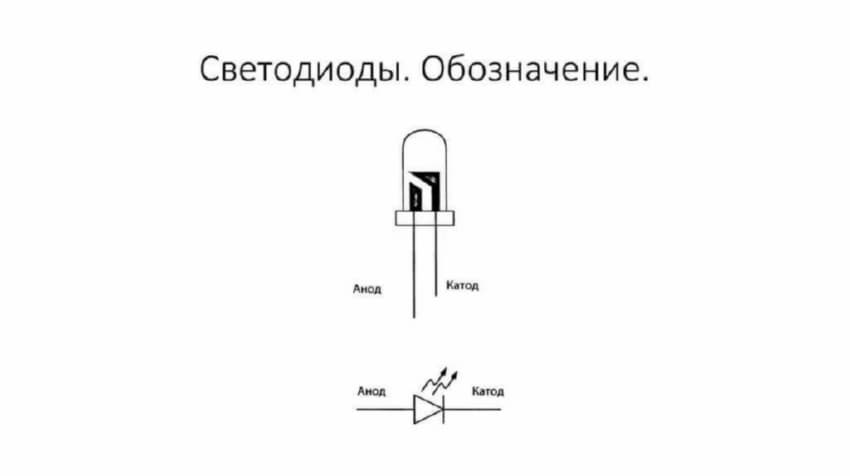
Електродите или краката на полупроводниковите и вакуумни електронни устройства също често се наричат анод и катод. Разгледайте условното графично обозначение на полупроводниковия диод в диаграмата:

Както виждаме, анодът на диода е свързан с положителната батерия. Това е така нареченото по същата причина - в този случай ток постъпва в изхода на диода във всеки случай. Истинският елемент на катода има лентова или точкова маркировка.
Светодиодът е подобен. На 5 mm светодиоди, вътрешността се вижда през колбата. Половината, която е по-голяма, е катодът.
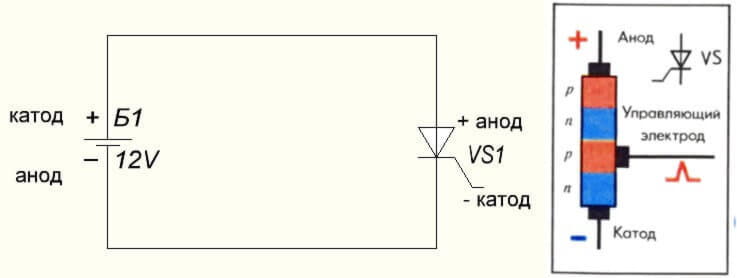
Ситуацията с тиристора също е същата: разпределението на пиновете и "еднополюсното" приложение на тези трикомпонентни компоненти го правят контролируем диод:
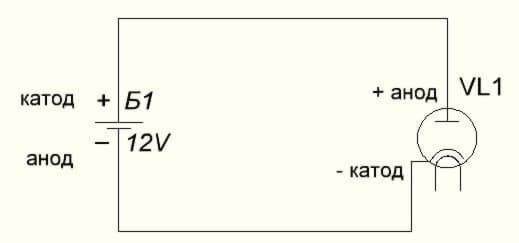
Във вакуумния диод анодът също се свързва с положителния, а катодът към отрицателния, което е показано на диаграмата по-долу. Въпреки че прилагането на обратното напрежение - имената на тези елементи няма да се променят, въпреки потока на електрически ток в обратната посока, макар и незначителен.
С пасивни елементи като кондензатори и резистори ситуацията е различна. Резисторът не отделя катода и анода, токът в него може да тече във всяка посока. Можете да дадете имена на заключенията му, в зависимост от ситуацията и разглежданата схема. В обикновени неполярни кондензатори. По-рядко, това разделяне с име на контакт се наблюдава в електролитни кондензатори.

заключение
Така че, да обобщим, отговаряйки на въпроса: как да си спомним къде е плюс, къде е минус на катода с анода? Налице е удобно мнемонично правило за електролиза, зареждане на батерии, галванични и полупроводникови устройства. Тези думи с подобни имена имат еднакъв брой букви, което е илюстрирано по-долу:
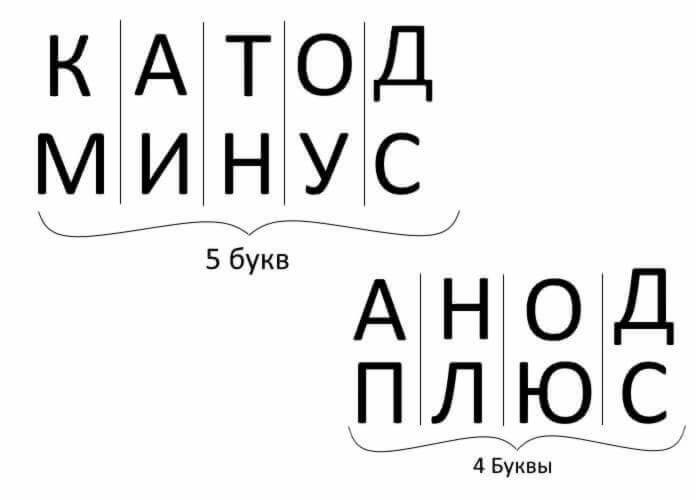
Във всички тези случаи токът тече от катода и се влива в анода.
Не се бърка от объркване: „Защо батерията има катод положителна, а когато се зарежда, става ли отрицателна?”. Не забравяйте с всички елементи на електрониката, както и с електролизерите и при галваничното покритие - като цяло, за всички потребители на енергия, изходът, свързан с плюс, се нарича анод. Това е мястото, където различията свършват, сега е по-лесно за вас да разберете какво е плюс, какво е отрицателно между изходите на елементите и устройствата.
Накрая Ви препоръчваме да гледате полезен видеоклип по темата на статията:
Сега знаете какви са анодите и катодите, както и как да ги запомните достатъчно бързо. Надяваме се, че предоставената информация е полезна и интересна за Вас!
Материали по темата:
- Каква е разликата между променлив ток и постоянен ток?
- Фазово и линейно напрежение в мрежата
- Как да зареждате батерията у дома